Рівняння стану ідеального газу (рівняння Менделєєва–Клапейрона). R = 8,31 . Для суміші газів стан кожного з них описується рівнянням Менделєєва–Клапейрона незалежно від інших. Закон Дальтона: тиск суміші газів дорівнює сумі парціальних тисків газів, що входять до складу суміші.
Тиск газу можна виразити через концентрацію газу та його абсолютну температуру: p =nkT. Модель реального газу, у якій нехтують розмірами молекул газу та їх взаємодією під час руху між зіткненнями, називають ідеальним газом. Рівняння Менделєєва — Клапейрона: pV = m RT/ M.
Решаем с помощью уравнения Менделеева – Клапейрона PV = m/M*R*T , перенесем объем V, в правую часть, получим P = m * R * T / V * M, масса разделить на объем = плотности: m / V = po, подставим и выразим плотность ро. p= (po)*R*T / M, po = p*M / R*T.
В физике плотность обозначают греческой буквой ρ (ро). плотность = масса объём ρ = m V , где m — масса, V — объём. Основной единицей плотности вещества является кг м 3 . Иногда используют единицу плотности г / см 3 .
В современном виде это уравнение записывают: pV = nRT, где p – давление, V – объем, n – количество вещества, T – температура.
Чтобы вычислить плотность какого-либо тела, нужно точно определить его массу и разделить её на точный объём этого тела.
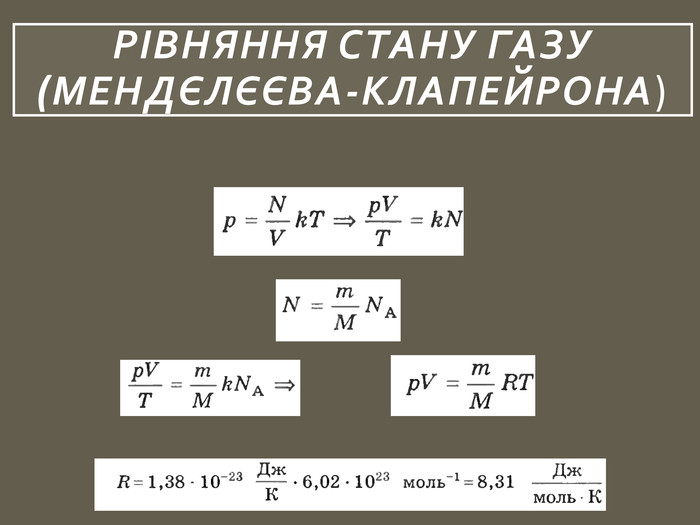

Для цього використовують рівняння стану ідеального газу (його також називають рівнянням Клапейрона-Менделєєва): PV = nRT. де. n – число молів газу; P – тиск …